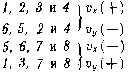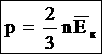- Главная
- Для учителя
- Архив заданий олимпиад по физике за 2009-2015 годы
- Владимир Анатольевич Зверев предлагает
- Несколько ссылок на работы Анатолия Шперха
- Общие вопросы методики обучения физике
- Статьи Александра Борисовича Рыбакова
- Важнейший общефизический принцип остается непонятым
- Рыбаков А. Б. Почитаем «Физику» вместе
- Рыбаков А.Б. Несколько замечаний о «Физике (ПС)», №10, 2015
- Рыбаков А.Б. О №12 «Физики (ПС)» и динамике автомобиля, или Спасут ли школу вузовские преподаватели?
- А.Б.Рыбаков Банджи-джампинг, сохранение импульса и уравнение Мещерского
- Рыбаков А.Б. О вращении Земли и всяком таком, или Удивительная физика в журнале «Физика (ПС)», №2/2015
- Экзамены
- Конспекты
- История физики
- Хронология физики
- Физики. Краткие биографии
- Дополнения к биографиям
- Нобелевские премии по физике
- История методики обучения физике
- Календарь на текущий год
- Физический календарь на 2026 год
- Физический календарь на 2025 год
- Календарь памятных дат в физике на 2023 год
- Юбилейные и памятные даты из истории физики в 2022 году
- Физический календарь на 2015 год
- Физический календарь на 2016 год. ч. 1
- Физический календарь на 2016 год. ч. 2
- Календарь памятных дат в физике на 2019 год
- Физики в Петербурге-Петрограде-Ленинграде
- Библиотека
- Медиатека
- О нас
Основное уравнение МКТ газов.
|
Основное уравнение МКТ газов |
|||||||
|
Модель идеального газа
|
|
||||||
|
Хаотичность молекулярного движения Проекции скоростей молекул на оси Ох и Оу положительны или отрицательны. |
|
||||||
|
Модель: идеальный газ. Задача: связать макроскопические параметры (то, что можно измерить) и микроскопические параметры (характеристики молекул), например давление и скорость движения молекул. Следствие опыта: давление газа объясняется ударами молекул о дно и стенки сосуда. Предварительное обсуждение:
|
|||||||
|
Определение |
Учет числа молекул (п.1) |
Причина - удары молекул (п.2) |
Удары абсолютно упругие(модель). |
||||
|
|
|
В проекциях:
|
|
||||
|
Предварительный итог:
|
|||||||
|
f - сила удара одной молекулы |
m0 - масса одной молекулы |
||||||
|
Учет расстояний (п.3) |
Подстановка |
Усреднение |
Общий итог: |
||||
|
|
|
Все направления равноправны:
В среднем |
|
||||
|
Это уравнение, выведенное впервые немецким физиком Р. Клаузиусом, называется основным уравнением молекулярно-кинетической теории идеального газа. Оно устанавливает связь между микроскопическими параметрами и макроскопическими (измеряемыми) величинами. |
|
||||||
|
Учитывая, что |
|
||||||
|
Давление идеального газа прямо пропорционально средней кинетической энергии поступательного движения молекул, содержащихся в единице объема газа. |
|
||||||
|
Т.к. |
|
||||||